Einige Metallhydroxide bilden in Wasser Laugen
Wir erinnern uns:
Nichtmetalloxide reagieren mit Wasser zu Säuren.
Wir werden jetzt sehen, dass Metalloxide in Wasser Laugen bilden.
Zunächst stellen wir ein Metalloxid her.
Wir werden Magnesium verbrennen und das entstehende Magnesiumoxid in destilliertes Wasser geben. Dazu entzünden wir ein Magnesiumband (Tiegelzange benutzen) über einem mit destilliertem Wasser halb gefüllten Becherglas.
2 Mg + O2 → 2 Mg2+O2- / exotherm
Magnesiumoxid ist eine salzähnliche Verbindung die aus Ionen besteht!
Jetzt lassen wir das Metalloxid mit Wasser reagieren.
Das entstehende Metalloxid [weißes Magnesiumoxid (Magnesia)] fällt ins Wasser. Es reagiert mit Wasser zunächst zu Magnesiumhydroxid, das in Wasser dissoziiert.
Mg2+O2- + H2O → Mg2+(OH-)2 → Mg2+(aq) + 2 OH-(aq)
Die entstandene Magnesiumlauge ist eine sehr schwache Lauge. Der Universalindikator ist für die wenigen Hydroxid-Ionen, die hier entstanden sind, viel zu unempfindlich. Ein wesentlich empfindlicherer Indikator ist Phenolphthalein.
Phenolphthalein ist ein Indikator, der bei Säuren farblos bleibt, sich bei Laugen jedoch rot färbt.
pH-Wert 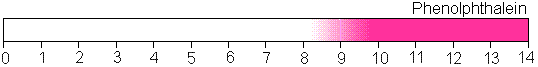

Die wässrige Lösung von Magnesium-Ionen und Hydroxid-Ionen heißt Magnesiumlauge.
Wir merken uns:
Einige Metalloxide reagieren mit Wasser zu Metallhydroxiden, die in Wasser Laugen bilden!



