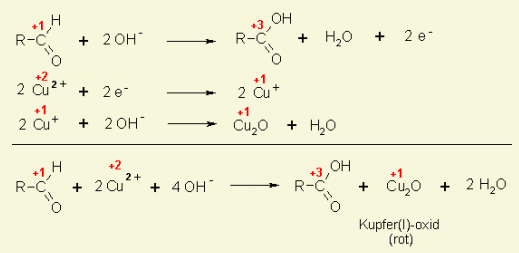
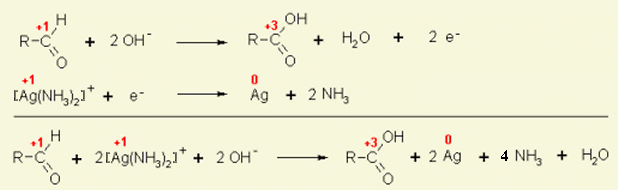
Fehlingprobe
Bei dieser sehr empfindlichen Nachweismethode werden zwei unterschiedliche Fehling-Lösungen gebraucht.
Zwei Lösungen:
Fehling I - Lösung:
Kupfer(II)-sulfatlösung
(7g CuSO4 • 5 H2O in 100 ml Wasser)
Fehling II - Lösung:
alkalische Tartratlösung
(34g KNaC4H4O6 • 4 H2O [„Seignettesalz“, ein Salz der Weinsäure] und 10g NaOH in 100 ml Wasser)

Anschließend wird das Reagenzglas mit dem Brenner oder im Wasserbad erwärmt. Danach gibt man eine kleine Probe eines Aldehyds hinzu.
Der beim Nachweis entstehende rote oder rotbraune Niederschlag besteht im Wesentlichen aus Kupfer(I)-oxid (Cu2O). Bei dieser Reaktion werden die Cu2+-Ionen zu Cu+-Ionen reduziert, das Aldehyd wird zu einer Alkansäure oxidiert.
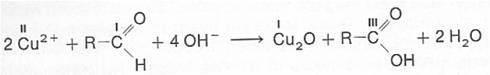
Bei der Fehlingprobe wird der Aldehyd mit Hilfe der Kupfer-Ionen des Kupfersulfates in einer alkalischen Lösung zu einer Carbonsäure oxidiert. Bei der Reaktion entsteht auch Kupferoxid mit seiner typischen rotbraunen Farbe.
Als Redoxreaktion:
- Quelle: Uni Regensburg; am 20.6.12 abgerufen - Hier findet man auch einen Film zum Versuch!
Der von Fehling (1812-1885) eingeführte Test kann auch zum Nachweis des Einfachzuckers Glucose im Blut (Blutzucker) verwendet werden, da dieser auch in der offenkettigen Aldehydform vorliegt. Hierbei wird die Glucose zu Gluconsäure oxidiert.