Esterspaltung
Ester können auf zwei unterschiedliche Arten wieder in die entsprechenden Carbonsäuren und Alkoholen gespalten werden:
Hydrolyse
Wie wir oben gesehen haben, ist die Veresterung eine säurekatalysierte Gleichgewichtsreaktion, bei der Wasser entsteht. Wenn wir nun einen Ester mit viel Wasser versetzen, eine katalytische Menge an Schwefelsäure zufügen und das ganze erhitzen, dann reagiert der Ester mit dem Wasser. Das Gleichgewicht wird zugunsten der Carbonsäure verschoben. Eine solche Reaktion nennt man Hydrolyse. Oder noch genauer: Eine Hydrolyse eines Carbonsäureesters in saurer Lösung.
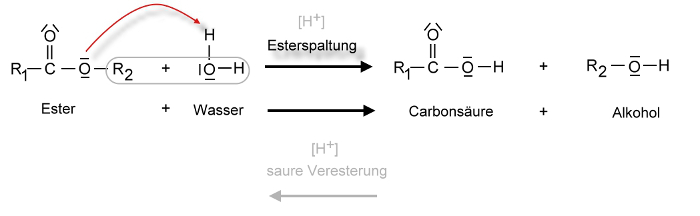
Reaktionsmechanismus der Hydrolyse eines Carbonsäureesters in saurer Lösung
Verseifung
Eine andere Art einen Ester zu spalten ist die Reaktion eines Esters mit einer Lauge wie z.B. Natronlauge. Hierbei entsteht der entsprechende Alkohol und ein Natriumsalz der zugrunde liegenden Carbonsäure. Der Begriff Verseifung kommt daher, dass Seifen Natrium- oder Kalium-Salze von Fettsäuren sind.








Kommentare
Die Mechanismuspfei le sind unvollständig bzw. falsch herum. Mir ist bewusst, dass das hier kein wissenschaftlic her Artikel sein soll, allerdings wäre es doch toll, Schülern von Anfang an zu zeigen wie das genau funktioniert, nämlich dass Pfeile im Mechanismus (also hier der Rote) immer den Elektronenfluss darstellen, hier also genau anders herum. Es muss ja nicht der komplette Mechanismus aufgezeigt werden (vielleicht aber eine Verlinkung für Interessierte? Hätte ich mir als Schüler auf jeden Fall angeguckt!).
Freut mich aber einen sehr engagierten Lehrer zu finden, der so eine Seite in seiner Freizeit betreibt.
mfg Quentin