Methan ist Hauptbestandteil des Erdgases
Erdgas ist ein ungiftiges, brennbares, farb- und in der Regel geruchloses Gas. Es ist leichter als Luft. Um eventuell austretendes Erdgas orten zu können, wird es mit einem Duftstoff versehen. Methan ist der Hauptbestandteil des Erdgases.
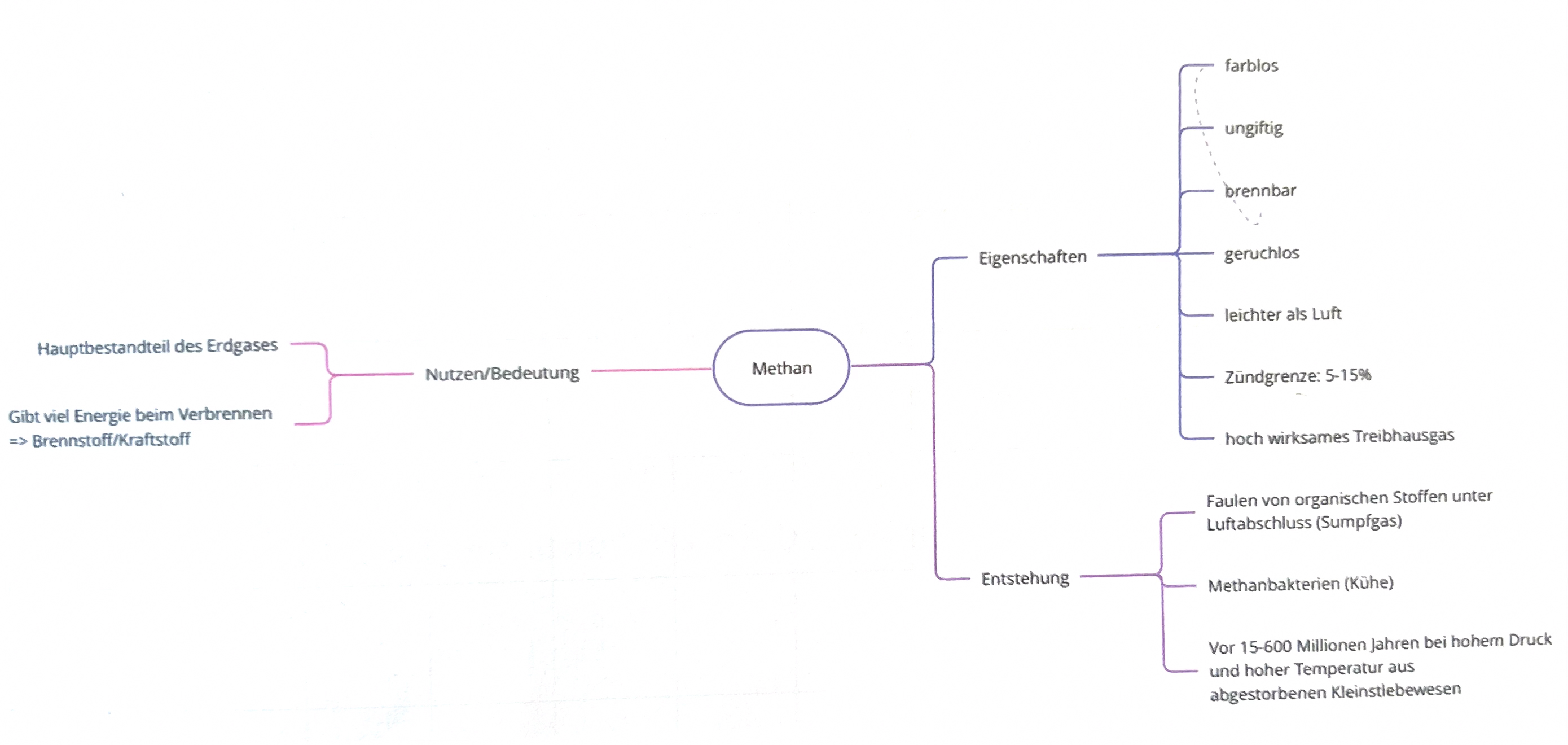
Entstehung des Erdgases
Erdgas entstand in tieferen Erdschichten bei hohen Temperaturen und Drücken im Laufe von 15 bis 600 Millionen Jahren aus abgestorbenen und abgesunkenen Kleinstlebewesen (Mikroorganismen, Algen, Plankton). Diese sind auf den Grund der damaligen Ozeane abgesunken und anschließend von undurchlässigen Schichten überdeckt worden. Der dann einsetzende chemische Prozess hat unser heutiges Erdgas gebildet, das auch bei vulkanischen Aktivitäten frei gesetzt wird.
Gefahren
Die Zündgrenze für Methan liegt bei 5 bis 15%. Mit anderen Worten: Sind in einem Raum mehr als 5 Volumenprozent Erdgas enthalten, so kann es durch einen Funken zur Explosion kommen.
Schlagendes Wetter:
Bergbauleute können auf eine Methanblase stoßen. Der Funke einer Spitzhacke kann schon zu einer Explosion führen. Eine Methangasexplosion im Bergbau wird auch als "schlagendes Wetter" bezeichnet.
Hausexplosion:
Eine defekte Gasleitung kann zum Ausströmen des Erdgases führen. Das Gas-Luftgemisch kann durch das Klingeln an der Haustür zur Explosion gebracht werden.
Methan ist ein hoch wirksames Treibhausgas!
Methan entsteht auch heute noch
Beim Faulen organischer Stoffe unter Luftabschluss in Sümpfen oder am Grund stark verschmutzter Gewässer bildet sich Sumpfgas, ein Gemisch aus Methan und Kohlendioxid.
Bestimmte Bakterien (Methanbakterien) können Methan herstellen. Der Verdauungstrakt von Wiederkäuern bietet ein besonders günstigen Lebensraum für solche Bakterien. Das so entstandene Biogas besteht überwiegend aus Methan (etwa 60 %) und Kohlendioxid (etwa 35 %), daneben enthält es noch Wasserstoff, Stickstoff und Schwefelwasserstoff.

[Bildquelle: sonderbar.twoday.net, Okt.2011]
Nutzen: Die Verbrennung
Bei der Verbrennung von Methan wird sehr viel Energie frei, die man sich zunutze machen kann: Laborbrenner, Gasherd, Gastherme, Autos, die mit Erdgas fahren usw.).
CH4 + 2 O2 → CO2 + 2 H2O / exotherm
Bei der Oxidation (Verbrennung) von Methan entsteht Kohlenstoffdioxid und Wasser(dampf). Dies ist übrigens bei der Verbrennung von allen organischen Verbindungen der Fall. Gleichwohl auch bei vielen organischen Stoffen auch noch andere Reaktionsprodukte entstehen können. Für den Fall einer Kerze hatten wir das schon im Anfangsunterricht besprochen.
Die Verbrennung von Methan hat energiepolitische Bedeutung. Diese Reaktion liefert viel Energie (Methan als fossiler Brennstoff).
Auf der anderen Seite ist das bei der Verbrennung entstehende Treibhausgas Kohlenstoffdioxid ein Grund für die globale Erwärmung unseres Planeten.
Wieso ist Methan leichter als Luft?
Dichteberechnung:
6 x 1023 Moleküle (= 1 mol) in rund 22 Liter (=Molvolumen, molares Volumen) [Gesetz von Avogadro]
Molekülmasse (Summe der Atommassen eines Moleküls) in unit. Zahl in Gramm entspricht 1 mol.
Molekülmasse von Methan = 16 u.
16 g Methan = 1mol befinden sich in 22 Liter Methan.
16 : 22 ~ 0,73 g
1 Liter Methan wiegt 0,73 g.
Vergleich: 1 Liter Luft wiegt 1,29 g
Methanhydrat
Methanhydrat ist im Prinzip gefrorenes Methan und kommt im Meer in großen Tiefen (hoher Druck) und tiefen Temperaturen vor. Dabei sitzen die Methanmoleküle im Kristallgitter des gefrorenen Wassers. Eine Erwärmung des Meerwassers, wie es infolge des Klimawandels zu beobachten ist, ließe das Methanhydrat schmelzen. Mikroorganismen im Meer würden dieses Methan nutzen und aus dem Methan Kohlenstoffdioxid produzieren. Hierfür würden sie den im Wasser gelösten Sauerstoff brauchen. Die Folgen wären:
1. Eine Ausbreitung von Meeresgebieten mit Sauerstoffmangel
2. Eine Freisetzung von Kohlenstoffdioxid aus dem Meer in die Atmosphäre
3. Eine Übersäuerung der Meere
Entweicht das Methan selbst aus dem Meer, so ist dies auch problematisch, da Methan ein hoch wirksames Treibhausgas ist.








