Stabilität und Geometrie der Peptidbindung
Aufgrund des nichtbindenden Elektronenpaares am Stickstoffatom und der Doppelbindung der Carbonyl-Gruppe haben wir es hier mit einem konjugierten System zu tun. Man kann dementsprechend mesomere Grenzformeln formulieren.
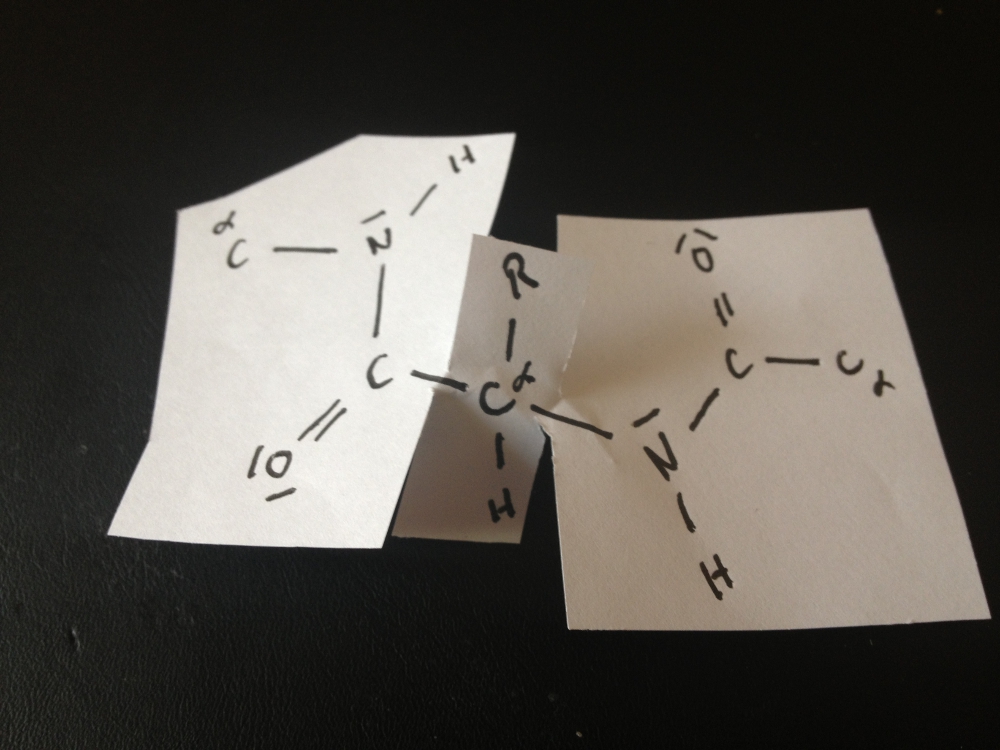
Hinweise zur Struktur links:
Die keilförmig gezeichneten Bindungen sollen verdeutlichen, dass die Bindungen räumlich zum Betrachter hin ausgerichtet sind. Die schraffiert gezeichneten Bindungen sollen verdeutlichen, dass die Bindungen vom Betrachter weg ausgerichtet sind. In der Strukturformeln sieht man dadurch auch deutlich, dass die Peptidbindung in einer Ebene liegt.
Aus den mesomeren Grenzformen ergeben sich zwei Konsequenzen:
- Die Peptidbindung ist eine recht stabile Bindung.
-
Die Peptid-Gruppe ist planar gebaut.Begründung für "Profis"
Grund für die planare Struktur der Peptid-Bindung ist nach dem VB-Modell die sp2-Hybridisierung von drei Atomen der Peptid-Gruppe, die in einem 120°-Winkel angeordnet sind. Die π-Elektronen sind über das Sauerstoff-, das Kohlenstoff- und das Stickstoff-Atom der Peptid-Gruppe delokalisiert. Damit ist die Bindung zwischen dem Kohlenstoff-Atom und dem Stickstoff-Atom nicht mehr frei drehbar. Eine Drehbarkeit ist nur noch an den α-Kohlenstoff-Atomen möglich. So können die beiden α-Kohlenstoff-Atome zur Kohlenstoff-Stickstoff-Bindung in cis- oder trans-Stellung stehen. Bei den natürlichen Proteinen liegt immer die trans-Form vor.