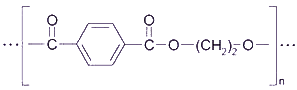
Kunststoffe, die beim Erhitzen schmelzen
Thermoplaste können bei Raumtemperatur verschieden hart sein. Diese Eigenschaft hängt mit der Struktur dieser Kunststoffe zusammen:
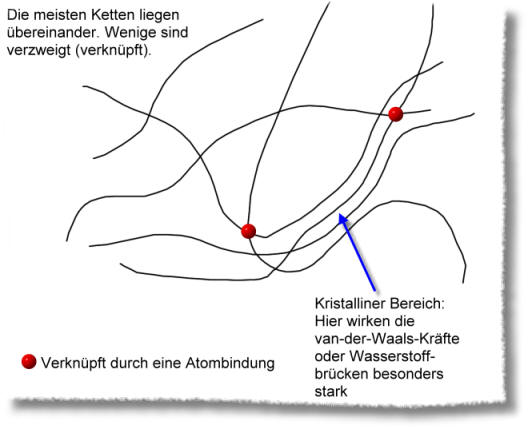
Thermoplaste, die bei Raumtemperatur weich sind, bestehen überwiegend aus ungeordneten, zum Teil verknäuelten Molekülketten mit relativ niedrigen mittleren Molekülmassen (ab 8000 u), die wie Spaghetti über- und untereinander liegen. Thermoplaste mit sehr langen Molekülketten (Molekulargewicht: bis 300 000 u) sind zähplastisch oder spröde, da die van-der-Waals-Kräfte viel größer sind.
Bei denjenigen Thermoplasten, die bei Raumtemperatur eher fest sind, liegen die Polymer-Ketten zudem in manchen Bereichen parallel zueinander. Solche Stellen nennt man kristalline Bereiche. Die anderen Bereiche nennt man amorph. Durch die größeren Berührungsflächen bei paralleler Anordnung in den kristallinen Bereichen, wirken hier die van-der-Waals-Kräfte besonders stark. Der Grad der kristallinen Bereiche ist einer der wichtigsten Faktoren für die Härte des Kunststoffes.
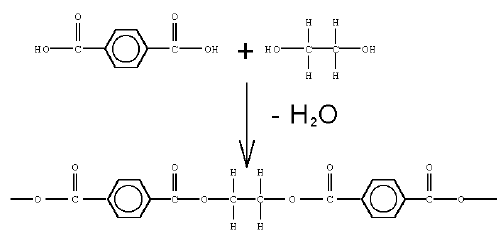
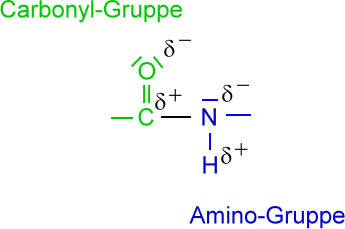
Bei manchen Thermoplasten, die polare funktionelle Gruppen aufweisen, können in diesen kristallinen Bereich zusätzlich Dipol-Dipol-Wechselwirkungen oder Wasserstoffbrücken zur Wirkung kommen. Gerade die Wasserstoffbrücken sind für die Festigkeit mancher Hochpolymere (z.B. Polyamide) ausschlaggebend.
Es können auch einige Kettenverknüpfungen durch Atombindungen vorhanden sein (wie z.B. beim Polyethen [PE]).
Auch die Zugfestigkeit von Fasern in Zugrichtung hängt vom Grad der kristallinen Bereiche ab. Diese kristallinen Bereiche können durch Überdehnen von Polymeren ausgelöst werden.
Entsprechend der Struktur eines Thermoplasts ist das Verhalten beim Erhitzen etwas unterschiedlich:
Prinzipiell geraten die Moleküle bei der Temperaturerhöhung in Schwingung und können schließlich die van-der-Waals-Kräfte überwinden: Die Zugfestigkeit nimmt ab, der Kunststoff wird weicher und plastisch verformbar und kann in Formen gegossen oder gepresst werden. Nach dem Erkalten erhält man ein festes thermoplastisches Formteil.
 Thermoplaste werden beim Erhitzen plastisch und lassen sich verformen. Nach dem Erkalten behalten sie ihre Form. Bei der Herstellung wird daher ein Extruder oder eine Spritzgießmaschine verwendet.
Thermoplaste werden beim Erhitzen plastisch und lassen sich verformen. Nach dem Erkalten behalten sie ihre Form. Bei der Herstellung wird daher ein Extruder oder eine Spritzgießmaschine verwendet.
Amorphe Thermoplaste (z.B. PVC) sind unterhalb der sogenannten Glastemperatur fest und glasartig transparent. Diese Temperatur ist keine exakte Temperatur, sondern ein Temperaturbereich, was ein Hinweis darauf ist, dass die Makromoleküle unterschiedliche Kettenlängen besitzen (Gemische gehen in einem Temperaturbereich in einen anderen Aggregatzustand über, Reinstoffe bei einer exakten Temperatur). Beim Erreichen der Glastemperatur wird der Kunststoff erst elastisch (thermoelastisch) dann, beim Erreichen der Erweichungstemperatur, plastisch (thermoplastisch). Erhitzt man den Thermoplast weiter, so geht er in eine zähflüssige, dann dünnflüssige Schmelze über, bevor er sich schließlich bei der Zersetzungstemperatur zersetzt. Amorphe Thermoplaste sind bei Gebrauchstemperatur meistens glasklar, hart, spröde und steif.
Teilkristalline Thermoplaste (z.B. Polypropen, PP; Polyamid, PA) erweichen bei einem höheren Temperaturbereich als die amorphen Thermoplaste. Sie sind häufig undurchsichtig und bei Gebrauchstemperatur meistens zähfest, biegsam bis hart.
Vollständig kristalline Thermoplaste (z.B. hochkristallines Polyethen, HDPE) gehen bei einer exakten Schmelztemperatur in eine dünnflüssige (hoch viskose) Schmelze über.
Die Quellbarkeit durch Lösemittel und die Lichtdurchlässigkeit nehmen mit zunehmend kristalliner Bereiche ab, da amorphe Polymere größere Lücken zwischen den Molekülketten besitzen als teilkristalline oder sogar kristalline Polymere. In diese Lücken kann das Lösemittel eindringen. Die größeren Lücken sind auch der Grund dafür, dass vermehrt Licht durch das Material gelangen kann.





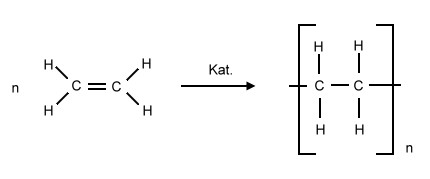



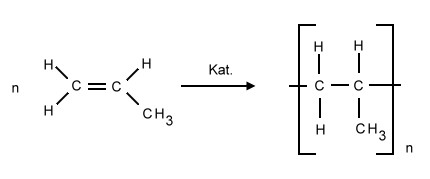
 Polypropen (Polypropylen, PP) ist ein teilkristalliner Thermoplast, der durch katalytische Polymerisation gewonnen wird.
Polypropen (Polypropylen, PP) ist ein teilkristalliner Thermoplast, der durch katalytische Polymerisation gewonnen wird. 


 Die ersten brauchbaren synthetischen Kunstfasern waren Polyamide. Sie zählen heute noch zu den mengenmäßig bedeutsamsten Kunstfasern. Wichtige Vertreter sind
Die ersten brauchbaren synthetischen Kunstfasern waren Polyamide. Sie zählen heute noch zu den mengenmäßig bedeutsamsten Kunstfasern. Wichtige Vertreter sind 

 Struktur
Struktur