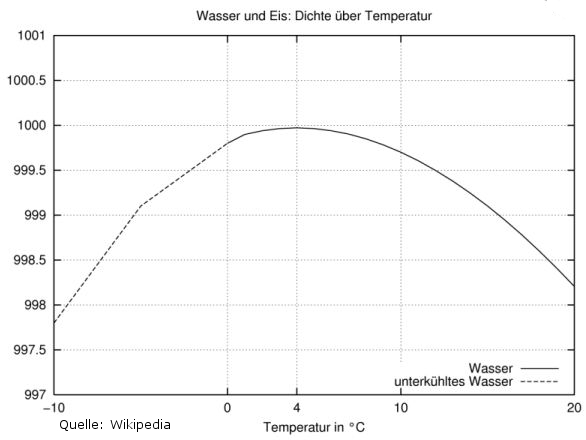
Dichte-Anomalie des flüssigen Wassers
Bei fast allen Stoffen nimmt die Dichte beim Erwärmen ab, da sich die Stoffe normalerweise beim Erwärmen ausdehnen.
[Bild]
Nur bei Wasser steigt die Dichte beim Erwärmen von 0°C auf 4°C zunächst etwas an und beginnt erst dann zu sinken.
Dieser Umstand ist lebensnotwendig für das Leben in Gewässern, denn das 4°C kalte Wasser sinkt nach unten. Die Gewässer können dadurch im Winter nicht vollständig durchfrieren und die Wassertiere in der Nähe des Gewässerbodens können dort überleben.



